Le nuove terapie anti-HCV, ovvero… come dibattersi tra aspettative dei pazienti, etica professionale, farmacoeconomia e linee guida
Secondo le stime più recenti l'infezione da virus dell'epatite C (HCV) interessa globalmente oltre 180 milioni di soggetti, circa il 3% della popolazione mondiale.
Data la frequente asintomaticità (fino al 90% dei casi) della sua fase acuta, rappresenta spesso un riscontro occasionale che avviene solo in fase di malattia cronica, che rappresenta la sua logica evoluzione nel 50-90% dei casi portando negli stadi terminali fino alla cirrosi epatica più o meno compensata e all'epatocarcinoma.
La storia naturale dell'infezione da HCV è pesantemente impattata dalla mancanza di un vaccino disponibile nonché dalle frequenti manifestazioni extra-epatiche (crioglobulinemia, linfoma non-Hodgkin, glomerulonefrite membranosa, porfiria cutanea tarda etc.), che la rendono a tutti gli effetti una malattia sistemica. D'altra parte, a differenza di quanto avviene per l'epatite B, l'eradicazione dell'infezione da HCV rappresenta un obiettivo ormai perseguibile: il raggiungimento della risposta virologica sostenuta (SVR) nel tempo dopo opportuna terapia si associa infatti ad avvenuta risoluzione dell'epatite in oltre il 99% dei casi.
Rispetto a 25 anni fa (l'HCV è stato infatti scoperto e caratterizzato solo nel 1989) la terapia dell'epatite cronica C ha compiuto passi di gigante, poiché in questo lasso di tempo il tasso di SVR con lo Standard of Care (SoC) disponibile al momento è passato dal 5-10% dei primi anni '90 ad oltre il 90% di oggi (Figura 1), indipendentemente dalla tipologia di paziente, quindi ivi compreso quello più difficile come il cirrotico con genotipo 1 non-responder a precedenti trattamenti. In particolare, negli ultimi 3-4 anni abbiamo assistito a una significativa produzione (e introduzione nella pratica clinica) di nuovi farmaci, e quindi di aggiornate linee guida, che hanno determinato cambiamenti epocali nell'approccio al paziente con epatite cronica C. Così, fino al 2010-11 il SoC era rappresentato invariabilmente dall'associazione interferone pegilato (PegIFN) + ribavirina (RBV), che assicurava un tasso di SVR variabile dal 40% del genotipo 1 all'80% del genotipo 2, a fronte però di un'elevata incidenza di effetti collaterali invalidanti ed anche gravi. Nel 2012-13, l'avvento dei primi farmaci ad azione antivirale diretta (DAAs), gli inibitori della proteasi (IP) di HCV boceprevir e telaprevir da impiegare in associazione a PegIFN + RBV, ha permesso di elevare il tasso di SVR, limitatamente ai pazienti con infezione da genotipo 1, al 70-80%, ma sempre a fronte di un'elevata incidenza di effetti collaterali, per certi versi ancor più invalidanti e gravi.
Figura 1 - Evoluzione della risposta virologica sostenuta alle varie terapie anti-HCV disponibili nel tempo (Legenda: G, genotipo - IFN, interferone – R, ribavirina – Peg, interferone pegilato – IP, inibitori della proteasi – DAAs, agenti antivirali diretti – m, mesi)
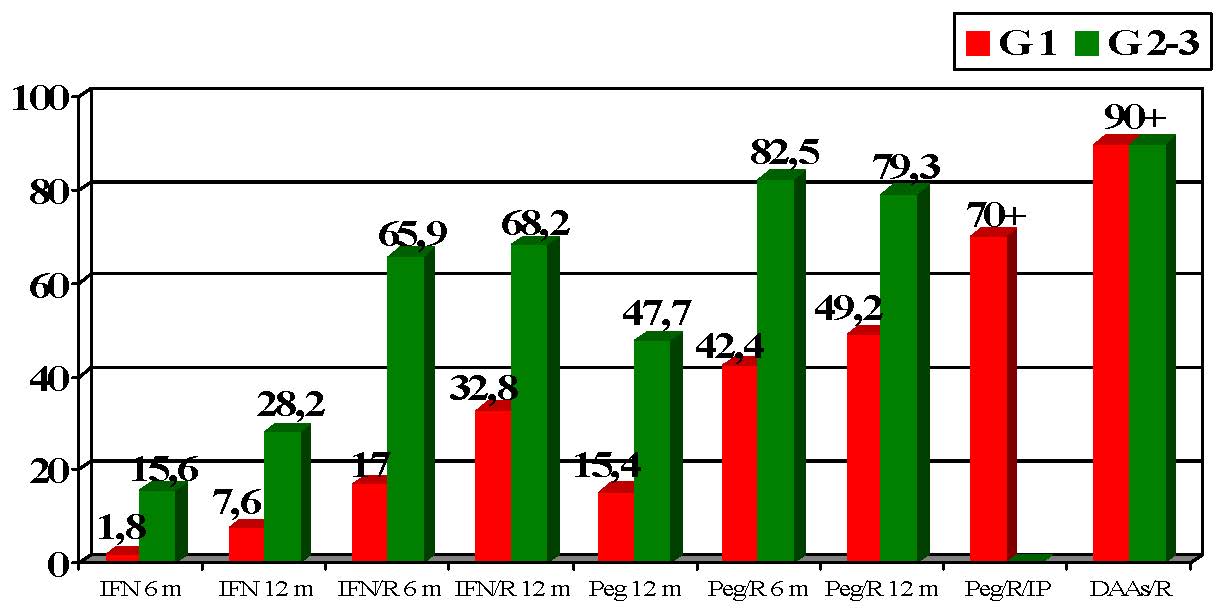
Dal 2014 la disponibilità di IP di seconda generazione e di altre categorie di DAAs (inibitori della polimerasi virale e dell'NS5A) ha permesso di aumentare invariabilmente a oltre il 90% i tassi di SVR praticamente in tutte le categorie di pazienti, allo stesso tempo abbreviando la durata del trattamento anche a sole 12 settimane e riducendo sensibilmente la frequenza e la gravità degli effetti collaterali grazie all'introduzione di schemi terapeutici interferon-free. Si può così affermare che l'unico reale "effetto collaterale" dei nuovi farmaci anti-HCV è rappresentato dal loro alto costo, non sostenibile non solo da parte dei paesi a limitate risorse ma in parte anche da paesi industrializzati, come il nostro, in cui gli effetti della crisi economica si fanno tuttora sentire.
Il sofosbuvir, inibitore della polimerasi virale che è stato il primo dei nuovi DAAs a essere autorizzato sia in Nord America che in Europa, è stato infatti introdotto negli Stati Uniti al costo di 1.000 dollari al giorno, ossia 84.000 dollari per un ciclo terapeutico di 12 settimane, con l'indicazione all'uso senza alcun limite né criterio d'esclusione. In Germania e Francia il costo iniziale si è invece aggirato tra i 53.000 e i 62.000 euro ed in Gran Bretagna sulle 45.000 sterline, sempre per cicli di 12 settimane. In realtà, alcuni Paesi a limitate risorse (Birmania, Brasile, Egitto, India, Iran e Kenya) hanno "strappato" alla casa produttrice un prezzo inferiore ai 1.000 dollari, mentre è stato calcolato che il costo di produzione, sempre per un quantitativo di farmaco necessario a 12 settimane di terapia, sarebbe limitato a soli 100 dollari. In Italia il farmaco è stato introdotto a fine 2014 al costo iniziale di 45mila euro: questa cifra elevata ha spinto l'ente regolatorio nazionale a pubblicare un documento d'indirizzo teso a dare la priorità e a limitare la prescrizione dei due DAAs al momento disponibili (il sofosbuvir, appunto, e il simeprevir, IP di seconda generazione):
- ad alcune rare condizioni (pazienti in attesa di trapianto di fegato o con recidiva dopo il trapianto stesso, o con epatite cronica dopo trapianto di altro organo solido o di midollo, o pazienti con epatite cronica e gravi manifestazioni extra-epatiche tipo sindromi crioglobulinemiche o linfoproliferative a cellule B)
- ai soggetti con epatite più grave quali quelli con fibrosi severa (F3) o cirrosi (F4), sia essa compensata che in fase di scompenso sia pur iniziale.
Queste disposizioni comportano per il momento l'esclusione dalle nuove terapie dei soggetti con quadro patologico meno grave, ovvero con fibrosi assente (F0), lieve (F1) o moderata (F2), che però rappresentano sostanzialmente la maggioranza della popolazione HCV-infetta. Un altro fattore fonte di discussione, e quindi passibile di future modifiche, è rappresentato dall'assenza di qualsiasi limite d'età per la prescrizione dei DAAs, cosicché è attualmente possibile trattare cirrotici ottantenni ma non soggetti giovani con infezione più lieve e quindi destinata all'eradicazione con la terapia: la principale conseguenza di tutto ciò è che le aspettative dei malati e l'etica professionale da una parte, le considerazioni economiche e l'attenersi alle linee guida dall'altra, entrano in apparente conflitto tra di loro.
Bibliografia
- Choo QL, Kuo G, Weiner AJ, Overby LR, Bradley DW, Houghton M. Isolation of a cDNA clone derived from a blood-borne non-A, non-B viral hepatitis genome. Science 1989; 244: 359-62.
- El-Serag HB, Rudolph KL. Hepatocellular carcinoma: epidemiology and molecular carcinogenesis. Gastroenterology 2007; 132: 2557-76.
- Freeman AJ, Law MG, Kaldor JM, Dore GJ. Predicting progression to cirrhosis in chronic hepatitis virus infection. J Viral Hepat 2003; 10: 285-93.
- Backus LI, Boothroyd DB, Phillips BR, Belperio P, Halloran J, Mole LA. A sustained virologic response reduces risk of all-cause mortality in patients with hepatitis C. Clin Gastroenterol Hepatol 2011; 9: 509-16.
- Allison RD, Conry-Cantilena C, Koziol D, Schechterly C, Ness P, Gibble J, et al. A 25-year study of the clinical and histologic outcomes of hepatitis C virus infection and its modes of transmission in a cohort of initially asymptomatic blood donors. J Infect Dis 2012; 206: 654-61.
- World Health Organization. Guidelines for the screening, care and treatment of persons with hepatitis C infection. World Health Organization, April 2014.
- Obach D, Deuffic-Burban S, Esmat G, Anwar WA, Dewedar S, Canva V, et al. Effectiveness and cost-effectiveness of immediate vs. delayed treatment of HCV-infected patients in a country with limited resources: the case of Egypt. Clin Infect Dis 2014; 58: 1064-71.
- AASLD-IAS-IDSA. Recommendations for testing, managing, and treating hepatitis C. Revised Date: December 19, 2014.
- European Association for the Study of the Liver. EASL recommendations on treatment of hepatitis C - April 2014.
- Associazione Italiana per lo Studio del Fegato (AISF). Documento di indirizzo dell'Associazione Italiana per lo Studio del Fegato per l'uso razionale di antivirali diretti di seconda generazione nelle categorie di pazienti affetti da epatite C cronica ammesse alla rimborsabilità in Italia. Documento pubblicato online in data 17 dicembre 2014, aggiornamento del 24 febbraio 2015.
